Indhold
Andre sektionerBrint er det letteste element og har mange industrielle anvendelser, herunder oprettelse af hydrogenerede fedtstoffer til brug i køkkenet og produktion af kulbrinter fra kul. Det er en væsentlig del af vandmolekyler og kan adskilles med en lille mængde elektricitet. Du kan også producere brintgas ved hjælp af nogle aktive metaller og stærke syrer. Begge metoder er relativt enkle og giver dig mulighed for at opsamle brintgas.
Trin
Metode 1 af 2: Brug af vandforskydning med aktive metaller
Saml de nødvendige materialer. For at opsamle brint ved hjælp af reaktionen ved at blande en stærk syre med et aktivt metal skal du bruge: en Erlenmeyer-kolbe, en gummiprop, plastrør, destilleret vand, reagensglas, en stor beholder, 3 molær saltsyre (HCl) og magnesium- eller zinkpiller.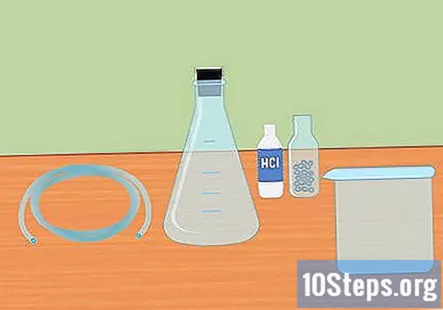
- En Erlenmeyer-kolbe er en glaskolbe, der har en konisk bund og cylindrisk hals.
- Gummiproppen er til toppen af kolben og skal have et hul i midten for at slangen kan gå igennem.
- Enten magnesium eller zink fungerer til dette eksperiment, du har ikke brug for begge dele.
- Nogle af disse forsyninger skal muligvis købes online eller i en laboratorieforsyningsbutik.

Bær passende beskyttelsesudstyr. Når du arbejder med en stærk syre som saltsyre, skal du sørge for at tage de rette sikkerhedsforanstaltninger. Det er vigtigt at bære en laboratoriekåbe, handsker, lukkede tåsko og øjenbeskyttelse.- Beskyttelsesbriller skal vikles omkring siderne af dine øjne for at beskytte dem mod stænk.
- Brug handsker, der passer ordentligt, så du opretholder en god fingerfærdighed i dine hænder og fingre.
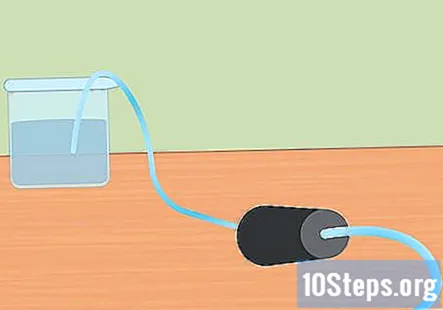
Forbered den eksperimentelle opsætning. Indsæt den ene ende af slangen i hullet i gummiproppen. Du vil have, at slangen skal gå helt igennem gummiproppen og stikke lidt ud fra enden. Fyld den store beholder med vand og placer den frie ende af slangen i vandet. Når eksperimentet begynder, lægger du gummiproppen i Erlenmeyer-kolben.- Læg disse stykker til side, indtil du er klar til at bruge dem.
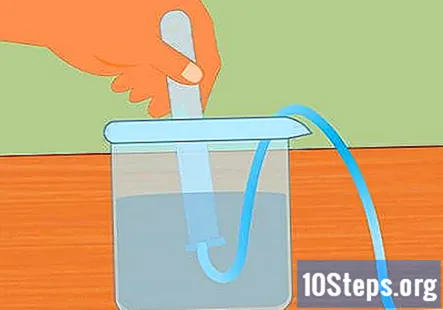
Sænk prøverøret ned i vandet. Tag mindst et reagensglas (du kan bruge mere, hvis du vil samle mere brint), og nedsænk det i vandet. Vip røret, så alle luftbobler kan slippe ud. Placer røret oven på det nedsænkede rør, der er fastgjort til gummiproppen i den modsatte ende.- Det er vigtigt, at alle luftbobler fjernes fra røret, inden du begynder. Hvis de ikke er det, vil gassen, der opsamles i røret, være mere end bare brint.
Tilsæt saltsyre til Erlenmeyer-kolben. Tilsæt nok saltsyre til at fylde kolben halvvejs. Ca. 100 ml skal være tilstrækkelig. Sørg for, at kolben er ren og tør, inden du tilsætter syren. Brug gummihandsker og vær forsigtig, når du fylder kolben.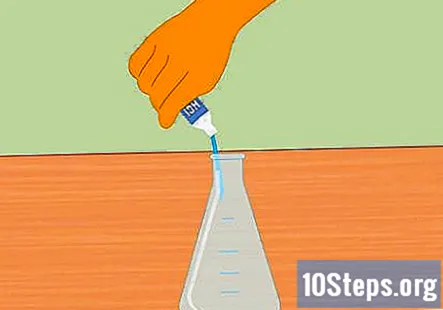
- Pas på ikke at spilde vand i syren. Vand tilsat syre kan føre til eksplosion og personskade.
Start den kemiske reaktion ved at tilføje metalpiller til HCI. Tilsæt en håndfuld zink- eller magnesiumpiller til saltsyren i kolben. Det nøjagtige beløb, du lægger i, er ikke vigtigt, men en lille håndfuld skal være nok til at starte reaktionen.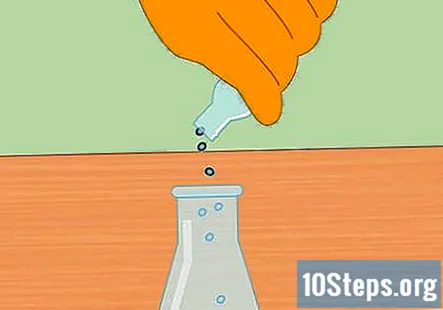
- Efter tilsætning af pellets, anbringes proppen i kolben, så systemet nu er lukket.
Opsaml brint i et nedsænket reagensglas. Når metallet reagerer med syren, dannes brintgas. Dette brint bevæger sig til toppen af kolben, gennem slangen og ind i reagensglasset nedsænket i vandet. Gassen vil fortrænge vandet, og du skal se en bobleform i toppen af reagensglas.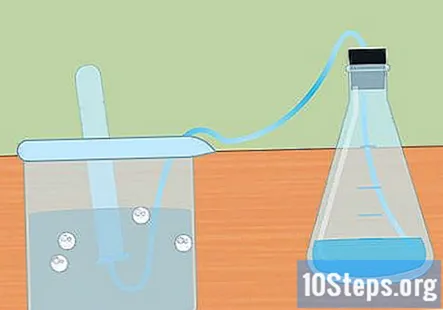
- Når reagensglas er fyldt med brint, nedsænk et andet rør med vand og placer det over slangen. Du kan indsamle så meget brint, som der produceres ved din reaktion.
- Hold prøverørene nedad for at forhindre, at brintgassen slipper ud i luften.
Bekræft, at gassen er brint. For at bekræfte, at gassen er brint, kan du gøre det, der kaldes skinne test. Tænd en tændstikker, og hold den under røret. Du vil høre en "pop" eller knirkende lyd, der indikerer, at der er brint til stede.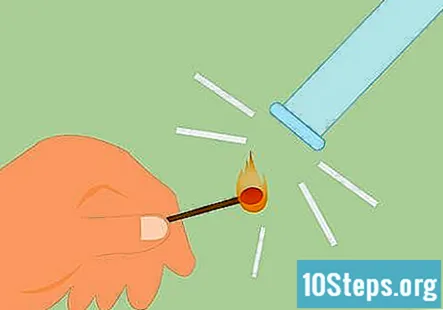
Metode 2 af 2: Brug af elektrolyse
Saml de nødvendige materialer. I dette eksperiment bruger du elektricitet til at adskille brint- og iltgasser fra vandmolekyler. For at opsamle brintgas ved hjælp af elektrolyse skal du bruge et 9-volts batteri, en blyant, to reagensglas, en plastbeholder, vand, bagepulver, to store elastikker (valgfrit) og en batteriklemme med klemmer i slutningen.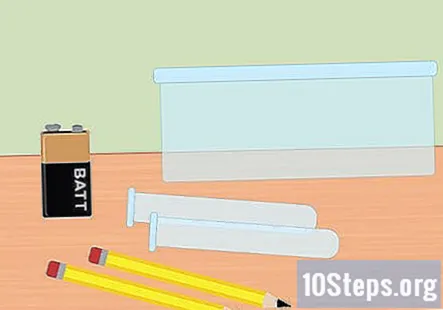
- Blyanten skal have grafit for at dette kan fungere. En blyant nummer 2 er perfekt. To små stykker grafit fungerer også til dette.
- En lille beholder eller skål til madopbevaring er tilstrækkelig.
- Sørg for, at batteriklemmen kan passe til et 9 volt batteri, og at den har en rød og sort ledning med alligatorklemmer i slutningen. Disse klemmer bruges til at tilslutte dit system til batteriet.
Fjern viskelæderet fra blyanten og del blyanten i halvdelen. Du har brug for to stykker grafit, en til den positive ende af batteriet og til den negative ende af batteriet. Slib begge ender af hvert stykke blyant til et punkt. Sørg for, at grafitten er godt eksponeret.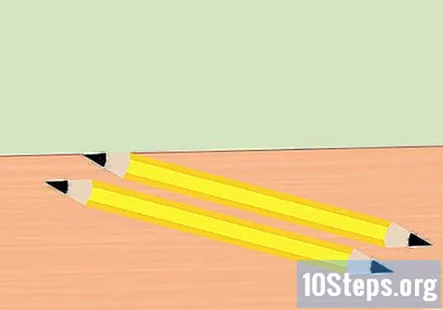
- Dette trin kan springes over, hvis du allerede har to stykker ren grafit.
Sæt 2 elastikker rundt om beholderen i en X-form. Dette trin er valgfrit, men er en nem måde at holde reagensglasene på plads, mens eksperimentet kører. Stræk et elastikbånd over beholderen og stræk et andet elastikbånd over det, så det krydser over det første og danner et X.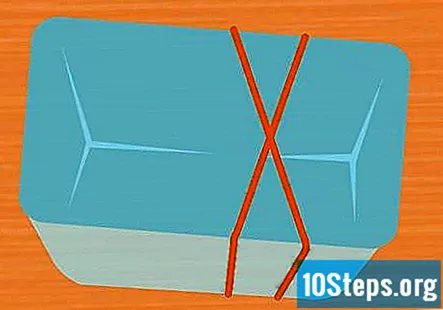
- Hvis du ikke bruger elastikker, skal du sørge for at fastgøre reagensglasene med tape eller snor, så de bliver på hovedet under eksperimentet.
Lav en bagepulver og vandopløsning. Opløsning af bagepulver i vand hjælper med at strømmen ledes i systemet. Den nøjagtige mængde bagepulver tilsat er ikke vigtig, men ca. 1 tsk pr. 1 kop vand skal være tilstrækkelig. Rør, indtil den er helt opløst.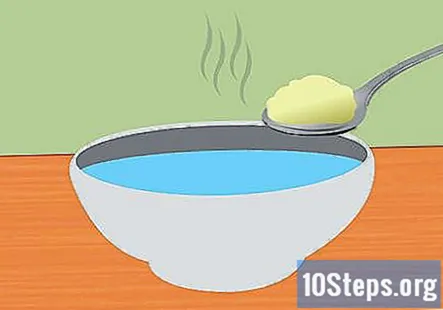
- Brug varmt vand til at fremskynde opløsningen af bagepulver.
Fyld plastbeholderen og reagensglas med bagepulveropløsningen. Beholderen skal være stor nok til at rumme begge reagensglas. Tilsæt nok af opløsningen til at fylde beholderen omkring tre fjerdedele fuld. Sænk prøverørene ned i opløsningen af beholderen, og vend dem på hovedet. Anbring hvert rør i kryds af gummibåndet X for at holde det på plads.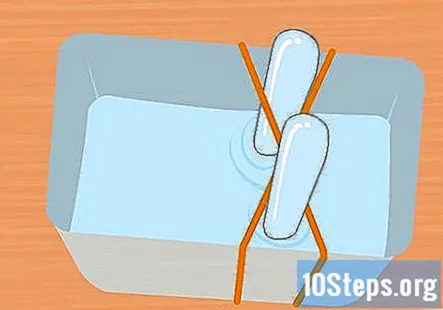
- Det er meget vigtigt, at begge reagensglas er helt fulde af vand, og at der ikke er nogen luftbobler tilbage.
Fastgør alligatorklemmerne til grafitten. Tag en klemme fra batteriklemmen og fastgør den til enden af en af blyanterne. Sørg for, at den rører så meget af grafitten som muligt. Gør det samme med den resterende alligatorklemme og blyantstykke.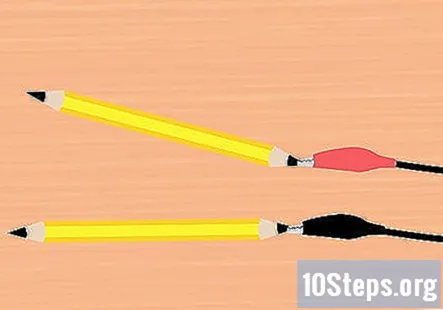
- En blyant skal fastgøres til den røde klemme og en blyant til den sorte klemme.
Skub den ikke fastspændte ende af blyanten ind i reagensglasset. Hold reagensglasset helt nedsænket, vip det let, så du kan skubbe den ikke fastspændte ende af blyanten ind i røret. Gentag denne proces med den anden blyant og den anden reagensglas.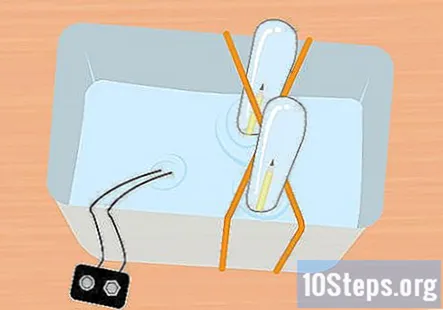
- På dette tidspunkt skal alt være under vandet, og der skal være et stykke blyant inde i hvert reagensglas.
- Hold enden af batteriklemmen, der er fastgjort til batteriet, ud af vandet.
Fastgør batteriklemmen til 9 volt batteriet. Med alt opsat er du nu klar til at anvende den strøm, der leveres af 9-volt batteriet. Enden af batteriklemmen skal stikke ud af beholderen, så klem batteriet på plads. Når batteriet er tilsluttet, skal du bemærke, at der stiger bobler fra enden af grafitten og flyder til toppen af hvert reagensglas.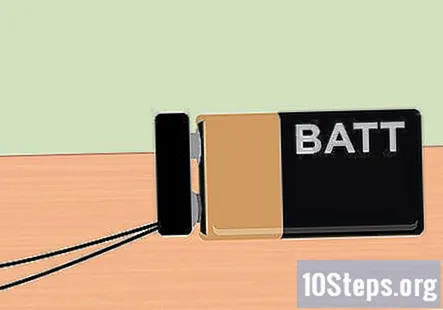
- Hvis du ikke kan se, at der produceres bobler, skal du kontrollere, om krokodilklemmerne er fastgjort til blyantens grafit. Kontroller også, at dit batteri er fuldt opladet.
- Testrøret med den negative ledning, der er fastgjort til blyanten, producerer brint, mens reagensglasset, der er fastgjort til batteriets positive ledning, producerer ilt.
Saml brint og ilt i de to reagensglas, indtil du har et par centimeter gas i hvert rør. Husk, at røret forbundet med den negative ende af batteriet har brint, og iltet er i røret forbundet med den positive ende. Fjern reagensglasene fra krukken en ad gangen. Hold dem på hovedet, og lad vandet løbe ud. Gassen i rørene forbliver, selvom du ikke kan se den.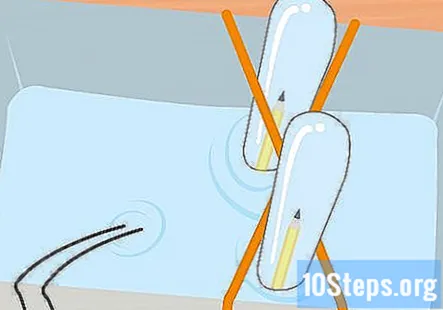
Test for tilstedeværelsen af brint. Du kan teste for tilstedeværelsen af brint ved at slå en tændstik og holde flammen op til gassen. Det giver en meget tydelig "knirkende pop" -lyd, hvis det er brint. Du kan også bruge et tændt lys i stedet for en tændstik.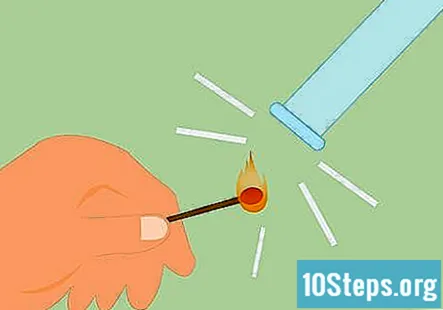
- For at teste for ilt i reagensglasset, der var forbundet med den positive side af strømkilden, skal du blæse en tændt tændstikker (eller et lys) ud og placere den stadig glødende ende under reagensglasset. Hvis lyset tændes igen, er der ilt til stede.
Fællesskabs spørgsmål og svar
Har jeg brug for to reagensglas, hvis jeg kun vil samle brint?

Miljøforsker Bess Ruff er en ph.d.-studerende i geografi ved Florida State University. Hun fik sin kandidatgrad i miljøvidenskab og ledelse fra University of California, Santa Barbara i 2016. Hun har gennemført undersøgelsesarbejde for havplanlægningsprojekter i Caribien og ydet forskningsstøtte som kandidat til Sustainable Fisheries Group.

Hvor meget brint kan der opsamles fra dette enkle eksperiment med elektrolyse? Og hvad ville være brintgasens tryk?
Det kommer an på. Reaktionshastigheden (opdeling af vand) er baseret på batteriets forstærkere og den tid, der er tilbage til at reagere. Normalt vil brintet være ved omtrent havets tryk, medmindre du gør eksperimentet i et rigtig varmt eller koldt miljø.
Hvorfor samler brintet sig i det negative rør
På grund af den måde, hvorpå vandmolekylerne deler elektroner, er hydrogenatomerne positivt ladede, og iltatomerne er negativt ladede. Når gasene trækkes ud, tiltrækkes det positivt ladede brint til det negative rør, mens det negativt ladede ilt tiltrækkes af det positive rør.
Hvorfor slap ikke gassen ud af mit gasopsamlingsrør?
Det er brint, en gas, der er lettere end alle andre, inklusive helium, hvilket betyder, at den forbliver i reagensglasset, så længe den lukkede ende af røret er på toppen, fordi de andre gasser fortrænger det. Årsagen til, at vi bruger helium i stedet for brint, er, at det ikke er brandfarligt. Dette skyldes, at det er en ædelgas (den har en fuld valensskal på 8 elektroner) og derfor ikke er reaktiv.
Ville gassen være meget brandfarlig?
Ja. Se Hindenburg-katastrofen på YouTube. Zeppelinerne brugte brint på grund af at det var den letteste gas og ret let at få. Det er også grunden til, at nogle bilproducenter arbejder på brintdrevne biler.
er dette den flydende form for brint?
Nej - brintet i dette eksperiment vil være gasformigt
Hvordan flydende brint? Svar
Advarsler
- Vær forsigtig med rent brint. Det er meget eksplosivt, når det blandes med luft.
- Sørg for, at al anden luft er fjernet fra det udstyr, hvor du opsamler brint.