Indhold
- etaper
- Metode 1 Afbalancering af en ligning med prøve- og fejlmetoden
- Metode 2 Equilibrer en ligning med den algebraiske metode
I kemi fastlægger en ligning, hvad der skete under en kemisk reaktion. Til venstre for ligningen placerer vi reagenserne, der blev brugt til eksperimentet og til højre de produkter, der blev opnået under eksperimentet. I henhold til princippet om konservering af massen (Lavoisier) under en kemisk reaktion, forsvinder intet atom, intet skabes, de kombineres forskelligt. I sammendrag skal du have det samme antal datomer for hvert element til højre som til venstre for ligningen. Det er derfor, en balance ligning altid skal være afbalanceret.
etaper
Metode 1 Afbalancering af en ligning med prøve- og fejlmetoden
-
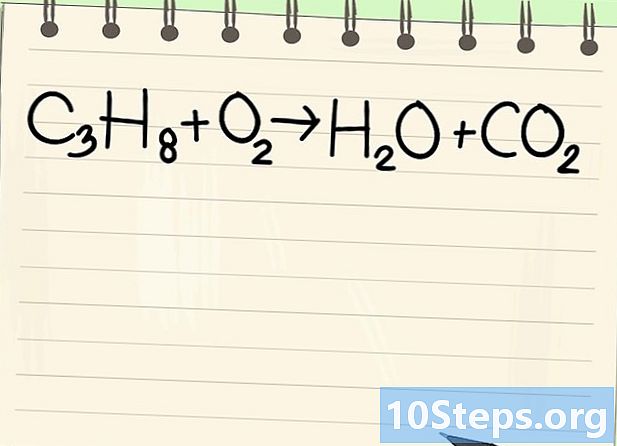
Bemærk balance ligningen. Vi behandler følgende ligning:- C3H8 + O2 -> H2O + CO2
- Dette er ligningen med propanforbrænding (C3H8) i ilt: vand og kuldioxid opnås.
-
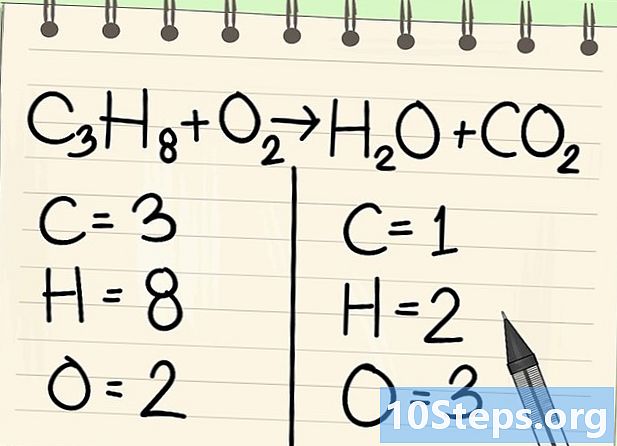
Tæl atomerne. Indtast antallet af datomer for hvert element på den ene side af ligningen og derefter det andet. For dette skal du tage hensyn til indekserne, hvis der ikke er nogen, er indekset 1.- Til venstre er der 3 carbonatomer, 8 brint og 2 ilt.
- Til højre er der 1 atom med kulstof, 2 brint og 3 ilt.
-
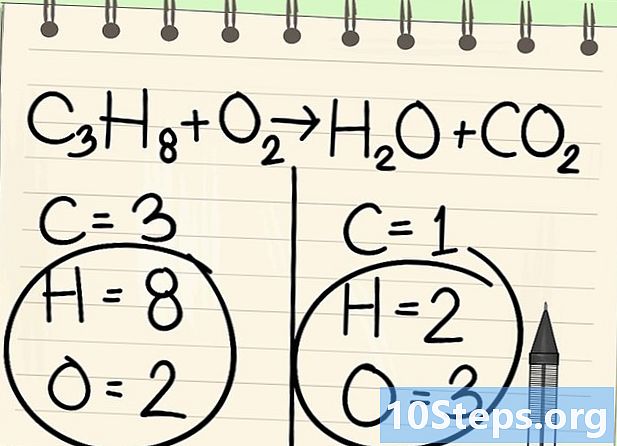
Efterlad øjeblikket brint og ilt. -

Begynd at balancere med det rigtige element. Vi starter altid med det i et molekyle før og efter reaktionen. Hvis der er flere, skal du tage den, der er monovalent i en af molekylerne. Her starter vi med carbonatomer. -

Balance kulstofatomer. Tilføj til højre en koefficient til kuldioxidmolekylet (CO2) hvori kulstoflatomet er alene. Vi sætter en 3 for at få de 3 venstre atomer.- C3H8 + O2 -> H2O + 3CO2
- Vi har således 3 carbonatomer til højre takket være koefficienten (3CO)2) og 3 carbonatomer til venstre takket være indekset (C3H8).
- I en ligning kan du placere alle de ønskede koefficienter, men du kan ikke røre ved sporene.
-
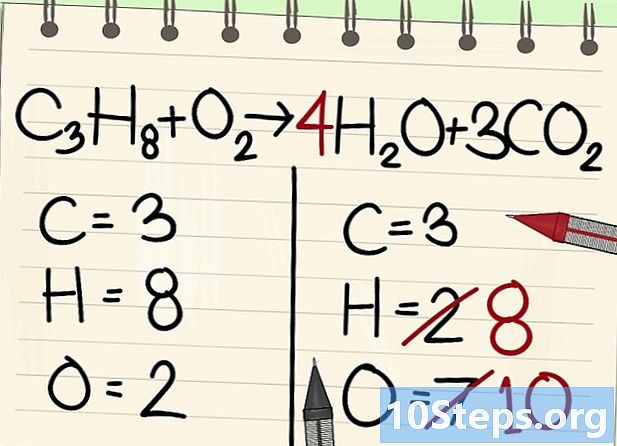
Balance brintatomerne. Da du har 8 tilbage af ligningen, har du brug for lige så meget ret.- C3H8 + O2 --> 4H2O + 3CO2
- Til højre vil du anbringe en koefficient på 4, fordi brintet er bivalent i vandmolekylet: indekset 2 indikerer, at to hydrogenatomer er forbundet.
- For at få antallet af hydrogenatomer til højre multiplicerer du koefficienten 4 med indekset 2 eller 8 atomer.
- Hvad angår iltatomerne til højre, er der nu 6 på den ene side, der kommer fra de tre molekyler af 3CO2 (3 x 2 = 6 atomer) og 4 fra de 4 molekyler af 4H2O (4 x 1 = 4 atomer), dvs. i alt 10 atomer ilt.
-
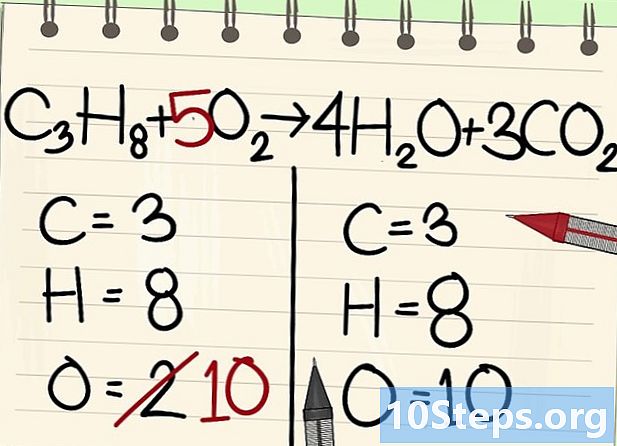
Balance atomerne af ilt.- På grund af kulstof- og brintbalancen er antallet af iltatomer ikke det samme på begge sider af ligningen. Vi så tidligere, at der var 10 atomer ilt til højre (4 fra vandmolekyler og 6 fra kuldioxidmolekyler). Til venstre er der kun 2 (fra O2).
- For at afbalancere ilt skal du tilføje en koefficient på 5 til det venstre iltmolekyle: du har 10 atomer ilt til venstre og den anden til højre.
- C3H8 + 5O2 -> 4H2O + 3CO2
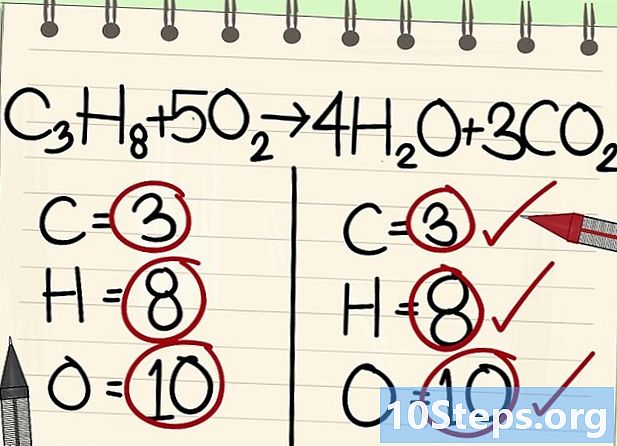
- Alle atomer (kulstof, brint og ilt) er afbalancerede: din ligning er afbalanceret.
Metode 2 Equilibrer en ligning med den algebraiske metode
-

Skriv ligningen til balance. Tildel hvert molekyle en bogstavelig koefficient. Vi kalder dem har, b, c og d. -
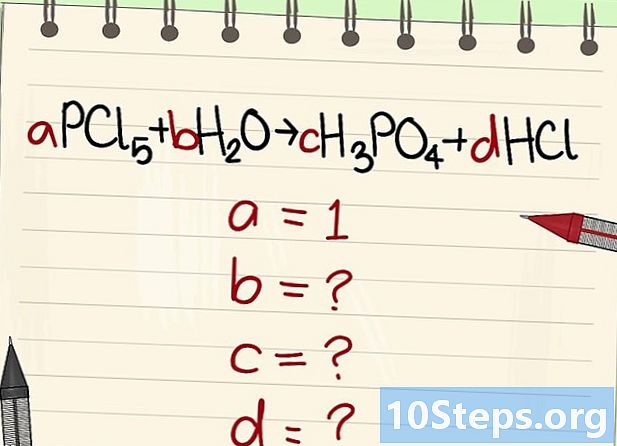
Find værdien af de andre bogstavelige koefficienter. Det vil vi spørge har = 1. -

Find sammenhængen mellem disse koefficienter. Ser man til venstre (reagenser) og højre (produkter), fastlægges forholdet mellem disse forskellige koefficienter.- Tag følgende ligning: aPCl5 + bH2O = cH3PO4 + dHCl. Det er blevet anført, at a = 1, hvilket betyder, at c = a, d = 5a og 2b = 3c + d. Udførte beregninger, c = 1, d = 5 og b = 4.

- Tag følgende ligning: aPCl5 + bH2O = cH3PO4 + dHCl. Det er blevet anført, at a = 1, hvilket betyder, at c = a, d = 5a og 2b = 3c + d. Udførte beregninger, c = 1, d = 5 og b = 4.