Indhold
Processen med at adskille atomkomponenter (brint og ilt) fra vand (H2O) ved hjælp af elektricitet kaldes elektrolyse. Dette er et yderst virkningsfuldt eksperiment, da de to gasser kan bruges isoleret, og brint er en af de største kilder til ren energi, som vi har adgang til. Selvom det synes vanskeligt, er elektrolyse relativt enkel. Du har bare brug for det rigtige udstyr, et godt kendskab til kemi og lidt dygtighed.
Steps
Del 1 af 2: Opsætning af udstyret
Fyld et 350 ml glas med varmt vand. Det er ikke nødvendigt at fylde det til randen. Efterlad lidt plads øverst. Varmen øger vandets elektriske ledningsevne, men eksperimentet skal også fungere, hvis det er koldt.
- Vandet kan enten være fra vasken eller fra flasken. Dette vil ikke påvirke eksperimentet.
- Det varme vand har en lavere viskositet, hvilket gør det muligt for de ledende ioner at bevæge sig mere frit.

Opløs en spiseskefuld (20 g) salt i vandet. Bare hæld saltet i glasset og rør det lidt for at fremskynde processen og omdanne vandet til en saltopløsning.- Natriumchlorid (eller simpelthen bordsalt) er en elektrolyt, der øger vandets ledningsevne, som ikke er en god leder alene.
- Ved at gøre vandet mere ledende vil batteristrømmen køre lettere og hjælpe med til at adskille brint og ilt.

Peg de to ender af to # 2-blyanter, indtil grafitten er godt synlig. Fjern om nødvendigt viskelæderne fra blyanterne. Tipene skal være skarpe nok til, at grafitten er fuldstændigt eksponeret på begge sider.- Grafitstængerne fungerer som elektroder og leder batteristrøm.
- Grafit er fantastisk til dette eksperiment, da det ikke opløses og ikke er beskadiget af vand.

Klip et stykke pap stort nok til at dække glasset. Vælg et ark, der er tykt nok til at forblive helt efter punktering. Prøv for eksempel at skære et firkantet stykke af en skoboks eller en anden tyk kasse.- Kartonen tjener til at holde grafitten i vandet væk fra siderne af glasset.
- Da papen ikke har nogen metalliske egenskaber, kan du placere den på glasset uden at påvirke eksperimentet.
Lav to huller med blyanterne i papen. Blyanterne skal passe perfekt i hullerne, så de ikke rykker eller glider. Brug derefter selve grafitspidserne til at gennembore pap. Eksperimentet stoppes, hvis grafitten berører bunden af glasset.
Del 2 af 2: Udførelse af eksperimentet
Forbind de to-leder ender med alligatorklips til batteripolerne. Batteriet er ansvarligt for at producere den elektriske strøm og alligatorens kløer til at transportere elektricitet til vandet. For at gøre dette skal du tilslutte et stik til den positive og en til den negative terminal.
- Det ideelle er at bruge et 6-volt batteri. Hvis du ikke kan finde et batteri af denne type, skal du bruge et 9-volt batteri.
- Batterier med denne spænding kan findes i næsten ethvert supermarked eller købmand.
Slut de andre ender af ledningerne til blyanterne. Forbindelserne skal være i direkte kontakt med grafitten. For at gøre dette skal du muligvis skrabe lidt mere af blyanttræet.
- Ved at udføre dette trin afslutter du forbindelsen mellem batteriet og grafitten, så den elektriske strøm kan køre til vandet.
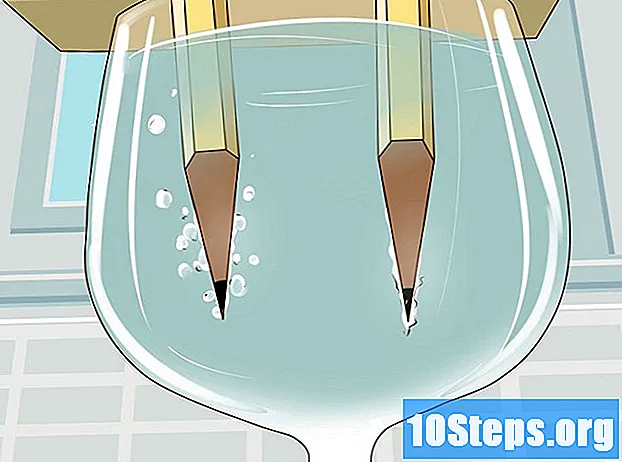
Placer papen over glasset, og dyb blyanterne ned. Gør dette forsigtigt, så blyanterne ikke bevæger sig for meget. Kartonstykket skal være godt afbalanceret i glassets munding.
- For at eksperimentet fungerer, er det meget vigtigt, at grafitten ikke berører glasset. Se godt på alle sider af glasset, og juster blyanterne.
Overhold separationen af brint og ilt. De neddykkede spidser af grafitten vil begynde at danne bobler i vandet, hvilket indikerer adskillelsen af de to gasser. Boblerne, der vises i slutningen forbundet til den negative terminal, er brint, medens boblerne, der dukker op omkring grafitten, der er forbundet til den positive terminal, vil være ilt.
- Kæden vil begynde at løbe gennem ledningen, så snart du tilslutter alligatorklemmerne til batteriet og grafitten.
- Mængden af hydrogenbobler vil være meget større, da vandmolekyler indeholder dobbelt så meget brint som ilt.
Tips
- Hvis du ikke finder grafitblyanter, skal du pakke to trådstykker rundt om batteripolerne og sæt ledningenes frie ender i vandet. Effekten vil være den samme som for blyanter.
- Prøv at bruge et batteri med en højere eller lavere spænding. Dette vil ændre intensiteten af den elektriske strøm, som igen vil påvirke molekylernes separationshastighed direkte.
Advarsler
- Elektrolytter, der bruges til at øge ledningsevnen, som salt, producerer en lille mængde klor, når de kommer i kontakt med vand. Det er ikke nok at gøre eksperimentet farligt, men du kan føle en let lugt af klor i luften.
- Bed en voksen om hjælp til at udføre dette eksperiment. Selvom risikoen er ret lille, er det altid muligt, at eksperimenter, der involverer gasser og elektricitet, går galt.
Nødvendige materialer
- To blyanter # 2.
- Et 6-volt eller 9-volt batteri.
- Et 350 ml glas.
- To ledninger med alligatorklips.
- En slibemaskine.
- Madlavning salt.